2. 超声医疗国家工程研究中心, 重庆, 401121
2. National Engineering Research Center of Ultrasound Medicine, Chongqing, 401121, China
高强度聚焦超声(High intensity focused ultrasound, HIFU)是一种体外无创治疗肿瘤技术,其核心是通过超声聚焦换能器将声能聚焦于靶组织使其发生凝固性坏死,却不损伤周围的正常组织[1]。当HIFU治疗位置较深或体积较大的肿瘤时通常需要较高的声功率(≥300 W)或较长的辐照时间,甚至重复治疗,因此焦前区或焦后区的生物组织经常发生一些诸如皮肤烧伤、肠道穿孔、骨膜疼痛等副作用[2-3],一般将其原因归结于超声热效应或换能器的设计缺陷。但是,空化效应产生的二次谐波及宽带噪声可被组织吸收并促进热量沉积,增强靶区或声通道组织的损伤[4]。因此,一方面,靶区可控的空化效应可用于HIFU增效及超声监控[5-6];另一方面,焦前区或焦后区的空化效应会造成额外的空化损伤,从而加重HIFU治疗的副作用[7]。可见,空化泡的空间分布与活动程度与HIFU疗效密切相关,而现有的空化研究主要集中于HIFU治疗中焦点处的生物组织,鲜有在脱气水中开展焦前区及焦后区的空化研究。
在超声波的正、负声压相的交变激励下,液体中的空化核周期性地生长与破裂的过程称为声空化[8],空化泡破裂瞬间,中心温度和压力分别高达5 000 K和1×105 kPa[9],其中,极端高温的出现引发光子向外辐射,即声致发光(Sonoluminescence, SL),也称为多泡声致发光(Multi-bubble sonoluminescence, MBSL)[10-11]。声致发光从光学角度实现了对空化泡的空间分布及活动程度的直观测量与分析[12-13],声致发光的强度在一定程度上可以反映声场中声压的分布,并依赖于声学参数(如声功率[14]、超声频率[15]及环境条件(如氧容量[16]、液体温度[17])等因素。目前,关于声致发光的研究一般都是基于低频(≤ 100 kHz)或低输出声功率(<100 W)的平面声场[13, 16, 18],相对而言,高强度聚焦超声场中声致发光的研究尚少。
因此,本文借助MBSL、被动空化检测(Passive cavitation detection, PCD)等手段在脱气水中研究了凹球面自聚焦超声换能器在不同声强下产生的聚焦声场中多泡的空间分布及活动程度,本研究的开展对人们认识焦前区、焦后区的副作用及优化HIFU治疗都有一定的指导意义。
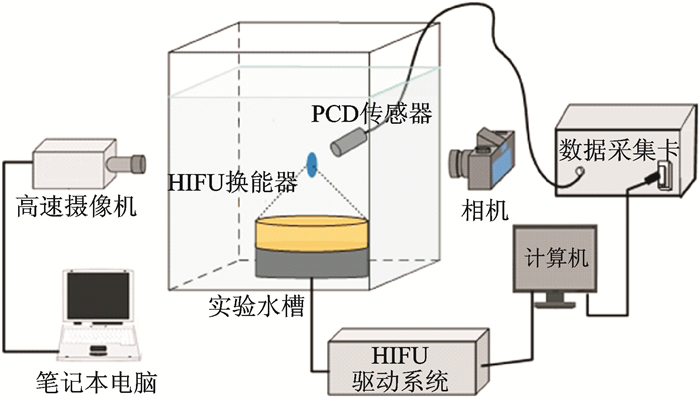
1 材料与方法 1.1 实验装置如图 1所示,本研究的实验装置主要由5部分组成:(1)HIFU治疗设备,由凹球面自聚焦超声换能器(工作频率为446 kHz,焦距与开口直径分别为150 mm和220 mm)、扫描运动装置(运动精度为0.1 mm)、计算机智能控制装置、脱气水处理单元与大功率电源构成;(2)高速摄像系统,包括日本Photron公司制造的FASTCAM SA4高速摄像机及v3.5.1 PFV软件;(3)被动空化检测系统,由美国泛美无损检测公司制造的V309-SU宽带聚焦换能器(中心频率5 MHz,焦距40 mm,开口直径13 mm),以及美国国家仪器有限公司生产的PXie-5122高速数据采集卡和v10.0.1 LabVIEW软件组成;(4)日本尼康公司制造的D3X数字相机;(5)光电倍增管系统,包括美国安捷伦科技有限公司制造的DSOX6004A数字示波器、自制电磁屏蔽箱、日本滨松公司制造的H10721光电倍增管和C6438-01信号放大器等。
|
图 1 实验装置示意图 Fig. 1 Schematic diagram of experimental set-up |
1.2 HIFU辐照
凹球面聚焦超声换能器被置于1个长和宽均为50 cm、高为100 cm的透明玻璃水槽中,固定换能器表面与水面的距离为230 mm,其中,实验使用的介质水需要经过严格的脱气处理,并保证氧容量为3.0 mg/L。实验开始,使用声功率计对HIFU换能器的输出声功率进行校验,通过美国ONDA公司制造的HFO-660光纤水听器进行声场扫描,测得-6 dB声焦域的长轴为14.1 mm、短轴为3.2 mm。然后,通过调节驱动电源的输出电压控制换能器的输出声功率在50~410 W之间(相邻声功率输出间隔为30 W),并通过式(1)算得不同输出声功率下的空间峰值声强Isp[19]为
| $ {I_{{\rm{sp}}}} = 1.56\frac{W}{{{L^2}}} $ | (1) |
式中:W为声功率;L=1.6 mm,为-6 dB声焦域的半高宽(Full width at half maximum, FWHM)。因此实验使用的声强范围为3 047~24 984 W/cm2,相邻声强间隔约为1 828 W/cm2。
1.3 被动空化检测首先,将中心频率为5 MHz的宽带聚焦换能器固定在垂直于HIFU声束轴向的方向上,使其焦点分别位于HIFU换能器的焦点处及焦点下方2 cm两个不同的位置。然后,通过数据线连接宽带换能器与高速数据采集系统,在不同声强下,采集HIFU辐照10 s期间两个不同位置的气泡散射的声信号,采样频率为20 MHz。然后,基于LabVIEW开发平台进行信号采集与去噪,其中,去噪是信号处理的关键环节[20],先通过Chebyshev带通滤波器读取所有信号,获取不同辐照时刻气泡散射声信号的频谱图,再将高次谐波和谐波周围±30 kHz的信号从频谱图中滤除。最后,采用式(2)计算3~6 MHz宽带噪声信号均方根RMS值[21],并绘出该值随时间变化的曲线。
| $ {\rm{RMS = }}\sqrt {\frac{1}{n}\sum\limits_1^n {y_i^2} } $ | (2) |
调节高速摄像机的位置使换能器的声焦域位于视野中央,在不同声强下,利用高速摄像系统拍摄聚焦声场中多泡的动态分布,其中,图像的帧频为1 000帧/s,分辨率为300像素每英吋(Pixels per inch, PPI)。调节Nikon相机的位置使聚焦声场的焦前区、焦点及焦后区均位于视野范围内,在暗室条件下拍摄MBSL的动态分布(拍摄参数:光圈F 2.8,曝光时间30 s,感光度H 2.0,图像分辨率为100 PPI)。
利用光电倍增管系统测量不同声强下聚焦声场的相对发光强度:在HIFU辐照过程中,将光电倍增管的感光口紧贴水槽玻璃外壁正对HIFU声焦域,声场中微弱的光信号被转换成电信号,通过信号放大器放大并在数字示波器上完成显示,其中,信号放大器的信号增益为500,控制电压为1.0 V。这里输出的电信号值与入射光子量成正比,因此可用于表征声场的整体发光强度,减去无HIFU辐照时的背景光强度,即得不同声强下聚焦声场整体的相对发光强度。
2 结果与讨论 2.1 不同声强下聚焦声场中多泡的动态分布气泡在声场中会产生两方面的结果:(1)气泡导致声波传播的衰减;(2)声辐射力推动气泡向焦点处聚集。不同声强下聚焦声场中多泡的动态分布情况如图 2所示。当声强较低时(如3 047 W/cm2),脱气水声场中的空化核呈驻波场模式分布,并位于驻波波腹处微弱振荡。提高声强(如8 531 W/cm2),聚焦声场的非线性效应显著,在声辐射力作用下声场中的气泡逐渐从驻波波腹处移向焦点处,如图 2可见气泡群呈“火苗”状聚集于焦点处,然后向焦后方生长,随即消失。气泡群周期性地出现、生长及消失的过程大约持续6 ms。进一步提高声强(如10 359 W/cm2),焦点处气泡群的出现、生长及消失这一过程的持续时间逐渐延长,气泡群的最大尺寸明显增大。当声强足够高时(如21 328 W/cm2),焦点处可见气泡群剧烈地抖动,同时发出连续的嘶嘶声。

|
图 2 不同声强下,聚焦声场中不同时刻的多泡分布情况 Fig. 2 Images of bubble activities at different acoustic intensities |
2.2 不同声强下聚焦声场中多泡的空化特征
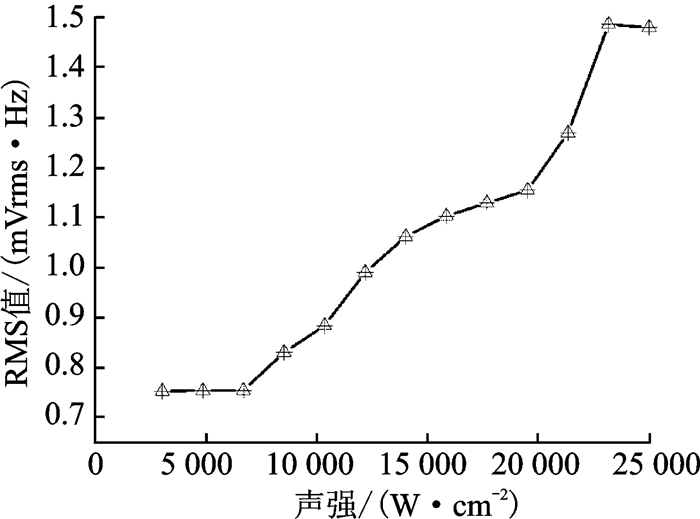
焦点处气泡在不同声强下散射的声信号的频谱图和3~6 MHz宽带噪声信号如图 3所示。当声强较低时(如3 047 W/cm2),频谱图中可见二次谐波与1/2次谐波,未见明显的3~6 MHz宽带噪声。通常1/2次谐波提示气泡在声波作用下的稳态空化,而非谐波的宽带噪声是瞬态空化发生的标志[4, 22]。由于空化是周期性的过程,因此在频谱图中空化信号呈周期性出现,在HIFU治疗中,通常需要结合空化信号分析凝固性坏死的形成机制。随着声强的逐渐提高(如8 531 W/cm2),高次谐波滋生,3~6 MHz宽带噪声的幅值显著增加。需要注意的是,宽带噪声的出现需要一定时间累积,这一过程是空化核在声波的持续作用下周期性地生长、崩溃形成气泡群的过程。进一步提高声强(如10 359 W/cm2),3~6 MHz宽带噪声出现需要的辐照时间缩短。当声强足够高时(如21 328 W/cm2),3~6 MHz宽带噪声不断地出现,气泡群的空化程度十分剧烈。图 4为焦点处3~6 MHz宽带噪声RMS值随声强的变化曲线,在一定声强范围内(3 047~ 24 984 W/cm2),3~6 MHz宽带噪声RMS值,即气泡群的空化程度与声强呈正相关。

|
图 3 不同声强下,焦点处某一时刻的空化信号频谱图及与之对应的3~6 MHz宽带噪声 Fig. 3 Cavitation signal spectrum and 3—6 MHz broadband emissions at focus under different acoustic intensities |
|
图 4 焦点处3~6 MHz宽带噪声RMS值随声强的变化曲线 Fig. 4 RMS of 3—6 MHz broadband at focus as a function of acoustic intensity |
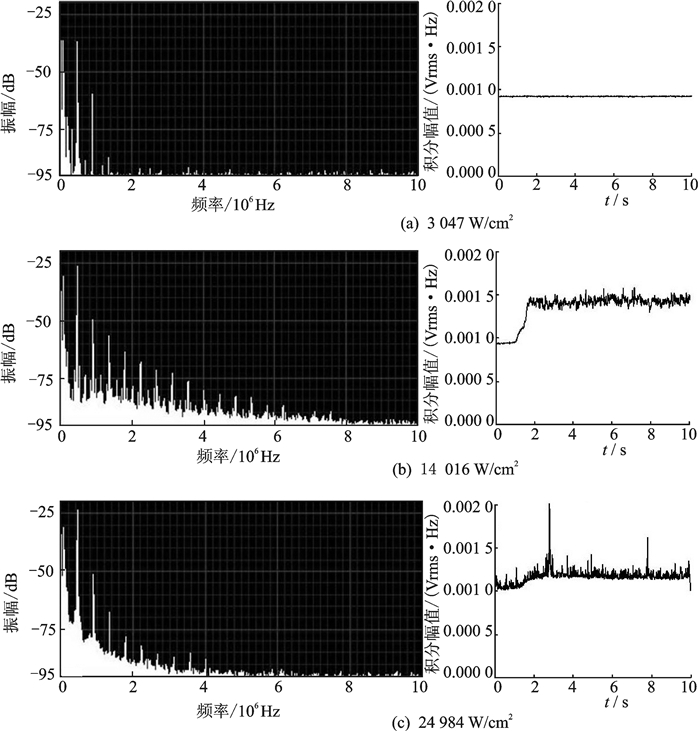
不同声强下,焦点下方2 cm处的空化信号频谱图及3~6 MHz宽带噪声如图 5所示。当声强较低时(如3 047 W/cm2),空化信号频谱图可见有1/2次谐波与二次谐波,无明显3~6 MHz宽带噪声。当声强为14 016 W/cm2时,高次谐波滋生,3~6 MHz的宽带噪声开始出现。当声强24 984 W/cm2时,3~6 MHz宽带噪声水平减弱,这是焦点处剧烈抖动的气泡群对焦前区以驻波场模式分布的气泡活动的影响导致的。
|
图 5 不同声强下,焦前2 cm处空化信号频谱图及其对应的3~6 MHz宽带噪声信号 Fig. 5 Cavitation signal spectrum and 3—6 MHz broadband emissions at 2 cm in front of focus at different intensities |
2.3 不同声强下聚焦声场中的多泡声致发光
不同声强下聚焦声场中的多泡声致发光的空间分布如图 6所示。当声强较低时(如3 047 W/cm2),虽然气泡分布于整个声场中,但并非所有气泡均可满足声致发光条件,发光主要集中在焦前区,并以驻波场模式分布。随着声强的逐渐提高(如3 047~10 359 W/cm2),焦前区满足发光条件的气泡不断朝换能器方向移动,由于焦前区及焦点处的气泡对超声能量的衰减作用导致焦后区的气泡在声强较低时难以发光。当声强为10 359~17 672 W/cm2时,焦点附近的发光范围及强度逐渐增大,因气-液界面的声波反射,焦后区域最终形成的发光区域呈“圆盘”状。当声强足够高时(如21 328 W/cm2),焦点处气泡群剧烈坍缩的同时发出连续的“嘶嘶”声,发光区域呈椭圆形,空化程度十分剧烈。

|
图 6 不同声强下多泡声致发光的空间分布 Fig. 6 Spatial distribution of MBSL at different acoustic intensities |
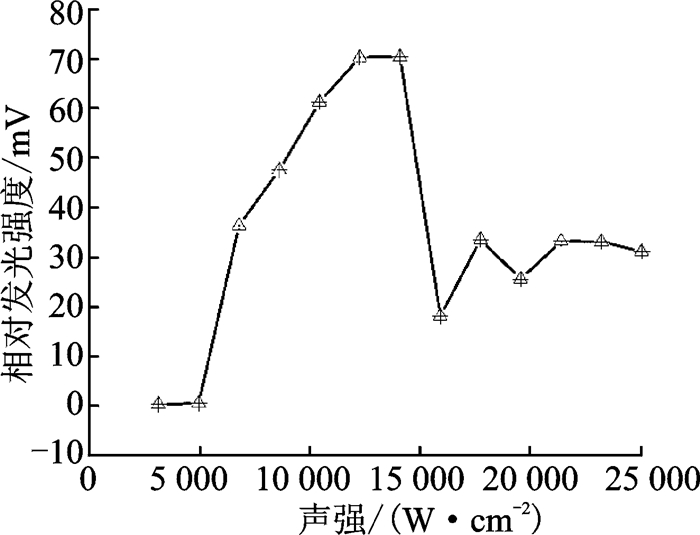
声场整体相对发光强度随声强的变化曲线如图 7所示。当声强较低时(3 047~4 875 W/cm2),声场整体相对发光强度较弱。当声强介于4 875与14 016 W/cm2之间时,声场整体相对发光强度与声强呈正相关,发光主要集中在焦前区。当声强超过14 016 W/cm2时,声场的相对发光强度出现减弱的趋势,随后变化不大,这是因为在较低的声强下,气泡主要位于驻波波腹处,相邻气泡距离较远,故气泡之间的相互作用力,即Bjerknes力较小。在较高的声强下,气泡发生聚集,气泡之间的距离缩短,Bjerknes力增强,该力不仅会促进气泡的融合,导致活化气泡数量减少[23],还会阻碍气泡的振荡,降低气泡崩溃产生的泡内温度,因此导致声场的整体相对发光强度大大减弱[24]。
|
图 7 声场整体相对发光强度随声强的变化曲线 Fig. 7 Overall relative MBSL intensity as a function of acoustic intensity |
3 结束语
聚焦超声在脱气水声场中MBSL的空间分布及发光强度与多泡的活动密切相关,当声强较低时(如3 047~10 359 W/cm2),气泡位于驻波波腹处,并呈驻波场模式分布,焦前区最先出现声致发光,发光范围逐渐朝换能器方向延展。在较高的声强下,气泡聚集于焦点处形成气泡群,气泡群的剧烈坍缩导致声场整体相对发光强度有所增强。当声强足够高时(如21 328 W/cm2),焦点处的气泡群剧烈抖动,高次谐波滋生,3~6 MHz宽带信号连续出现,提示空化程度十分剧烈,此时焦点处出现椭圆形亮斑,而气泡群的出现导致声场整体相对发光强度急剧减弱。
| [1] |
王智彪, 李发琪, 冯若. 治疗超声原理及应用[M]. 南京: 南京大学出版社, 2008. Wang Zhibiao, Li Faqi, Feng Ruo. The principle and application of treatment ultrasound[M]. Nanjing: Nanjing University Press, 2008. |
| [2] |
曾飚, 周敏, 华媛媛, 等. 高强度聚焦超声治疗子宫肌瘤的安全性分析[J]. 重庆医学, 2013, 42(4): 370-372. Zeng Biao, Zhou Min, Hua Yuanyuan, et al. The safety of high intensity focused ultrasound for treatment of uterine leiomyoma[J]. Chongqing Med, 2013, 42(4): 370-372. DOI:10.3969/j.issn.1671-8348.2013.04.004 |
| [3] |
汪伟, 刘文英, 周洁敏, 等. 高强度聚焦超声治疗症状性子宫肌瘤的初步临床研究[J]. 中华超声影像学杂志, 2002, 11(3): 161-163. Wang Wei, Liu Wenying, Zhou Jiemin, et al. Treatment of symptomatic uterine leiomyomata with high intensity focused ultrasound:A preliminary clinical study[J]. Chin J Utrasonogr, 2002, 11(3): 161-163. DOI:10.3760/j.issn:1004-4477.2002.03.009 |
| [4] |
刘珊. 空化效应和血流对脉冲HIFU消融治疗的影响[D]. 重庆: 重庆医科大学, 2015. Liu Shan. The influence of cavitation and blood flow on pulsed high intensity focused ultrasound ablation[D]. Chongqing: College of Chongqing Medical University, 2015. http://cdmd.cnki.com.cn/Article/CDMD-10631-1016008513.htm |
| [5] |
Clement G T. Perspectives in clinical uses of high-intensity focused ultrasound[J]. Ultrasonics, 2004, 42(10): 1087-1093. DOI:10.1016/j.ultras.2004.04.003 |
| [6] |
Kaneko Y, Maruyama T, Takegami K, et al. Use of a microbubble agent to increase the effects of high intensity focused ultrasound on liver tissue[J]. Eur Radiol, 2005, 15(7): 1415-1420. DOI:10.1007/s00330-005-2663-7 |
| [7] |
李非. 聚焦声场中的多泡分布及声致发光研究[D]. 重庆: 重庆医科大学, 2016. Li Fei. Study on multi-bubble dynamics and sonoluminescence in focused iltrasound field[D]. Chongqing: Chongqing Medical University, 2016. http://cdmd.cnki.com.cn/Article/CDMD-10631-1016782581.htm |
| [8] |
陈伟中. 声空化物理[M]. 北京: 科学出版社, 2016: 161-178. Chen Weizhong. Acoustic cavitation physics[M]. Beijing: Science Press, 2016: 161-178. |
| [9] |
Suslick K S, Flannigan D J. Inside a collapsing bubble:Sonoluminescence and the conditions during cavitation[J]. Annu Rev Phys Chem, 2008, 59(1): 659-683. DOI:10.1146/annurev.physchem.59.032607.093739 |
| [10] |
Putterman S J. Sonoluminescence:Sound into light[J]. Sci Am, 1995, 272(2): 46-51. DOI:10.1038/scientificamerican0295-46 |
| [11] |
Putterman S J, Weninger K R. Sonoluminescence:How bubbles turn sound into light[J]. Annu Rev Fluid Mech, 2000, 32: 445-476. DOI:10.1146/annurev.fluid.32.1.445 |
| [12] |
丁春峰, 邢达. 利用声致发光成像技术测量液体中的声场[J]. 压电与声光, 2004, 26(2): 152-154. Ding Chunfeng, Xing Da. Real time measurement of ultrosound field distribution in liquid with sonoluminescence imaging technology[J]. Piezoel Ectr Ics & Acou Stooptics, 2004, 26(2): 152-154. DOI:10.3969/j.issn.1004-2474.2004.02.021 |
| [13] |
Cao Hua, Yin Hui, Qiao Yangzi, et al. Sonochemiluminescence observation and acoustic detection of cavitation induced by pulsed HIFU at a tissue-fluid interface[J]. Ultrasonics Sonochemistry, 2013, 20(6): 1370-1375. DOI:10.1016/j.ultsonch.2013.03.002 |
| [14] |
Lee H B, Choi P K. Acoustic power dependences of sonoluminescence and bubble dynamics[J]. Ultrasonics Sonochemistry, 2014, 21(6): 2037-2043. DOI:10.1016/j.ultsonch.2014.02.008 |
| [15] |
Ashokkumar M, Lee J, Iida Y, et al. Spatial distribution of acoustic cavitation bubbles at different ultrasound frequencies[J]. Chem Phys Chem, 2010, 11(8): 1680-1684. DOI:10.1002/cphc.200901037 |
| [16] |
Liu Li, Yang Yang, Liu Peng, et al. The influence of air content in water on ultrasonic cavitation field[J]. Ultrasonics Sonochemistry, 2014, 21(2): 566-571. DOI:10.1016/j.ultsonch.2013.10.007 |
| [17] |
Didenko Y T, Nastich D N, Pugach S P, et al. The effect of bulk solution temperature on the intensity and spectra of water sonoluminescence[J]. Ultrasonics, 1994, 32(1): 71-76. DOI:10.1016/0041-624X(94)90083-3 |
| [18] |
Hatanaka S, Yasui K, Kozuka T, et al. Influence of bubble clustering on multibubble sonoluminescence[J]. Ultrasonics, 2002, 40(1/2/3/4/5/6/7/8): 655-660. |
| [19] |
He Min, Zhong Zhiqiang, Li Xing, et al. Effects of different hydrostatic pressure on lesions in ex vivo bovine livers induced by high intensity focused ultrasound[J]. Ultrasonics Sonochemistry, 2017, 36: 36-41. DOI:10.1016/j.ultsonch.2016.11.001 |
| [20] |
胡广书, 汪梦蝶. 生物医学信号处理研究综述[J]. 数据采集与处理, 2015, 30(5): 915-932. Hu Guangshu, Wang Mengdie. Survey of biomedical signal processing[J]. Journal of Data Acquisition and Processing, 2015, 30(5): 915-932. |
| [21] |
陈杰, 易华容, 王彬, 等. 高强度聚焦超声治疗中的空化及其与回声、热效应之间的关系[J]. 中国医学影像技术, 2009, 25(10): 1896-1898. Chen Jie, Yi Huarong, Wang Bin, et al. Cavitation and the relationship between cavitation, echo and the thermal effects of HIFU treatment[J]. Chin J Med Imaging Technol, 2009, 25(10): 1896-1898. DOI:10.3321/j.issn:1003-3289.2009.10.045 |
| [22] |
李成海. 超声激发高强度聚焦超声所致沸腾气泡散射声信号的研究[D]. 重庆: 重庆医科大学, 2015. Li Chenghai. Research on ultrasound-stimulated scattering signal from high intensity focused ultrasound-induced boiling bubbles[D]. Chongqing: Chongqing Medical University, 2015. http://cdmd.cnki.com.cn/Article/CDMD-10631-1016007263.htm |
| [23] |
Tervo J T, Mettin R, Lauterborn W. Bubble cluster dynamics in acoustic cavitation[J]. Acta Acoust, 2006, 92(92): 178-180. |
| [24] |
Stricker L, Dollet B, Rivas D F, et al. Interacting bubble clouds and their sonochemical production[J]. Acoust Soc Am, 2013, 134(3): 1854-1862. DOI:10.1121/1.4816412 |
 2018, Vol. 33
2018, Vol. 33

